L’air respirable à usage médical ne répond pas aux mêmes critères que l’air respirable industriel. Les gaz à usage médical, dont fait partie l’air médicinal, sont réglementés par la pharmacopée Européenne.
Cette dernière est directement opposable en France depuis le 01/10/97 (arrêté du 7/11/96) et remplace la pharmacopée Française dont seules subsistent quelques monographies en vigueur.
La norme NFS 90-140, (air à usage médical - Taux d’impuretés admissibles.....) qui servait de référence pour les contrôles jusqu’en 1998 est également remplacée par la pharmacopée Européenne.
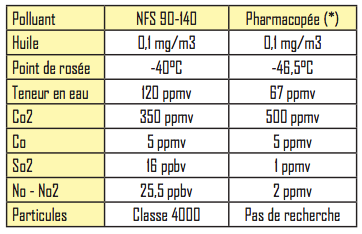
Les teneurs en polluants admissibles diffèrent, comme le montre le tableau ci-dessous :
 La teneur en humidité est essentielle afin d’éviter tout risque de condensation et de développement bactérien. La valeur indiquée s’entend à 1 atm, soit un point de rosée sous pression de -30°C environ à 7 bars.
La teneur en humidité est essentielle afin d’éviter tout risque de condensation et de développement bactérien. La valeur indiquée s’entend à 1 atm, soit un point de rosée sous pression de -30°C environ à 7 bars.
Il est à noter que la pharmacopée Européenne ne fixe aucune exigence en matière de particules ni de bactéries.
 L’air médicinal est un produit sans statut, il n’est pas considéré comme gaz médical ni comme gaz médicinal lorsqu’il est produit sur site (Station de compression d’air ambiant+ traitement) et n’est donc pas soumis à une autorisation de mise sur le marché (AMM).
L’air médicinal est un produit sans statut, il n’est pas considéré comme gaz médical ni comme gaz médicinal lorsqu’il est produit sur site (Station de compression d’air ambiant+ traitement) et n’est donc pas soumis à une autorisation de mise sur le marché (AMM).
Nos unités d’épurations Série BA (ci-contre) , répondent parfaitement aux teneurs admissibles en polluants exigées par la Pharmacopée Européenne. N’hésitez pas à consulter nos spécialistes pour toute information complémentaire sur ce sujet.
(*) Pharmacopée Européenne 2008 monographie 1238.
► Découvrir la gamme ICI


